原子结构与元素性质
电子排布式与轨道表示式
介绍电子排布式、简化电子排布式和轨道表示式的概念、书写规则和意义,包括实例和价层电子轨道表示式表格。
原子结构示意图、电子排布式、电子排布图
价层电子排布式书写规则是处于稳定状态的原子,核外电子将尽可能地按能量最低原理排布
| 核外电子排布的表示方法 | 意义 | 实例(以硫原子为例) |
|---|---|---|
| 原子结构示意图 | 表示每个能层容纳的电子数 | 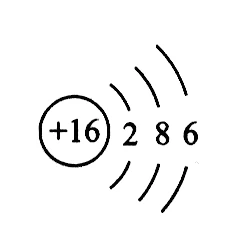 |
| 电子排布式 | 表示每个能级容纳的电子数 | |
| 简化的电子排布式 | 前一周期稀有气体元素符号 | |
| 电子排布图(轨道表示式) | 表示每个原子轨道容纳的电子数 | 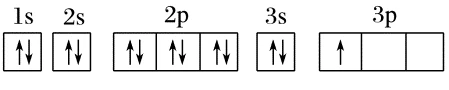 |
孤电子对和价层电子对辨析
| 辨析对象 | 意义 | 实例 |
|---|---|---|
| 孤电子对 | 在分子或原子团中,未参与成键的成对价电子 | 如 |
| 价层电子对 | 在分子或原子团中,中心原子的价层电子对 = σ 键电子对 + 孤电子对 | 如 |
部分元素电子排布式和价层电子轨道表示式
| 原子序数 | 元素名称 | 元素符号 | 电子(或简化电子)排布式 | 价层电子轨道表示式 |
|---|---|---|---|---|
| 1 | 氢 | |||
| 2 | 氦 | |||
| 3 | 锂 | |||
| 4 | 铍 | |||
| 5 | 硼 | |||
| 6 | 碳 | |||
| 7 | 氮 | |||
| 10 | 氖 | |||
| 11 | 钠 | |||
| 12 | 镁 | |||
| 13 | 铝 | |||
| 14 | 硅 | |||
| 18 | 氩 | |||
| 19 | 钾 | |||
| 20 | 钙 | |||
| 21 | 钪 | |||
| 22 | 钛 | |||
| 23 | 钒 | |||
| 24 * | 铬 | |||
| 25 | 锰 | |||
| 26 | 铁 | |||
| 27 | 钴 | |||
| 29 * | 铜 | |||
| 30 | 锌 | |||
| 31 | 镓 | |||
| 32 | 锗 | |||
| 33 | 砷 | |||
| 36 | 氪 | |||
| 37 | 铷 |
*特殊情况:
,
过渡金属阳离子
过渡金属阳离子失去电子时从最外层电子开始失去: