分子空间结构与物质性质
分子的极性 手性分子
讲解共价键的极性和非极性、分子的极性判断方法,包括向量和和快速判断,以及手性分子的概念。
共价键的极性
- 共价键有 极性共价键 和 非极性共价键
极性共价键:由不同原子形成的共价键,电子对会发生偏移(向电负性大的一侧偏移)。极性键中的两个键合原子,一个呈正电性(),另一个呈负电性( )。在极性共价键中,成键原子吸引电子能力的差别越大,共用电子对偏移程度越大,共价键的极性越强
非极性共价键:电子对不发生偏移的共价键因此,电负性差值越大,极性越大
特别:
的 电负性不同,之间形成极性共价键;但由于其极性微弱,它在四氯化碳中的溶解度高于在水中的溶解度 - 分子可分为 极性分子 和 非极性分子
- 极性分子的正电中心和负电中心不重合,使分子的某一个部分呈正电性(
),另一部分呈负电性 ( ) - 非极性分子的正电中心和负电中心重合
- 极性分子的正电中心和负电中心不重合,使分子的某一个部分呈正电性(
分子的极性的判断
判断分子的极性可依据分子中化学键的极性的 向量和
- 只含非极性键 的分子一定是非极性分子
如:
- 含极性键的分子有没有极性,必须依据分子中极性键的极性的 向量和是否等于零 而定。当分子中各个键的极性的向量和等于零时,是非极性分子,否则是极性分子
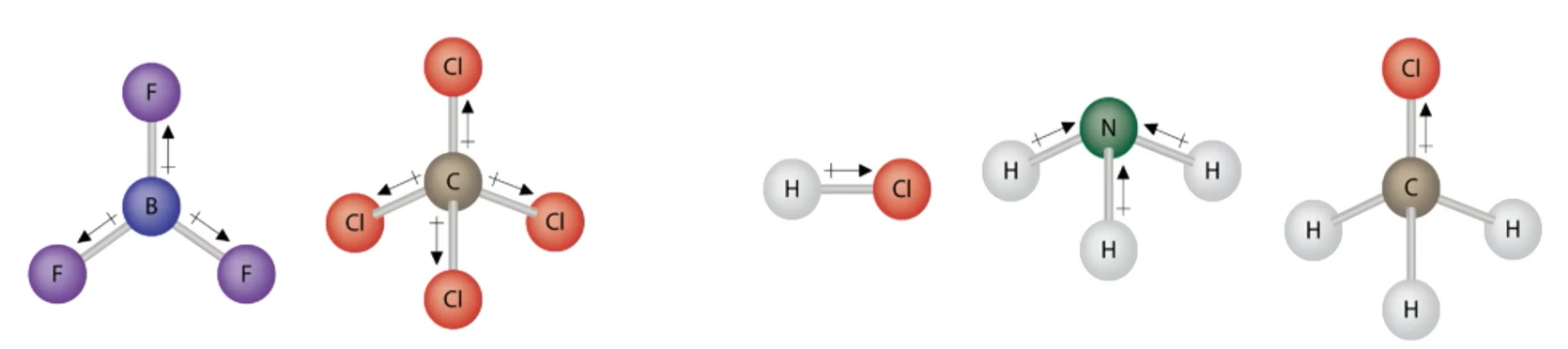
- 也可以根据 分子的正电中心和负电中心是否重合 来判断它是否是极性分子
快速判断方法:
- 化合价法:
型分子中,中心原子的化合价的绝对值 等于 该元素的价电子数 时该分子为非极性分子,此时分子的空间结构对称;若中心原子的化合价的绝对值不等于其价电子数,则分子的空间结构不对称,其分子为极性分子,具体实例如下: 分子 中心原子的化合价的绝对值 该元素的价电子数 分子极性 非极性 非极性 非极性 非极性 极性 极性 极性 - 根据分子所含键的类型及分子立体构型判断
分子所含原子个数 键的极性 键角 立体构型 分子极性 单原子: 非极性分子 双原子: 非极性键 直线形 非极性分子 双原子: 极性键 直线形 极性分子 三原子: 极性键 形 极性分子 三原子: 极性键 直线形 非极性分子 四原子: 极性键 平面正三角形 非极性分子 四原子: 极性键 三角锥形 极性分子 五原子: 极性键 正四面体形 非极性分子 五原子: 极性键 四面体形 极性分子 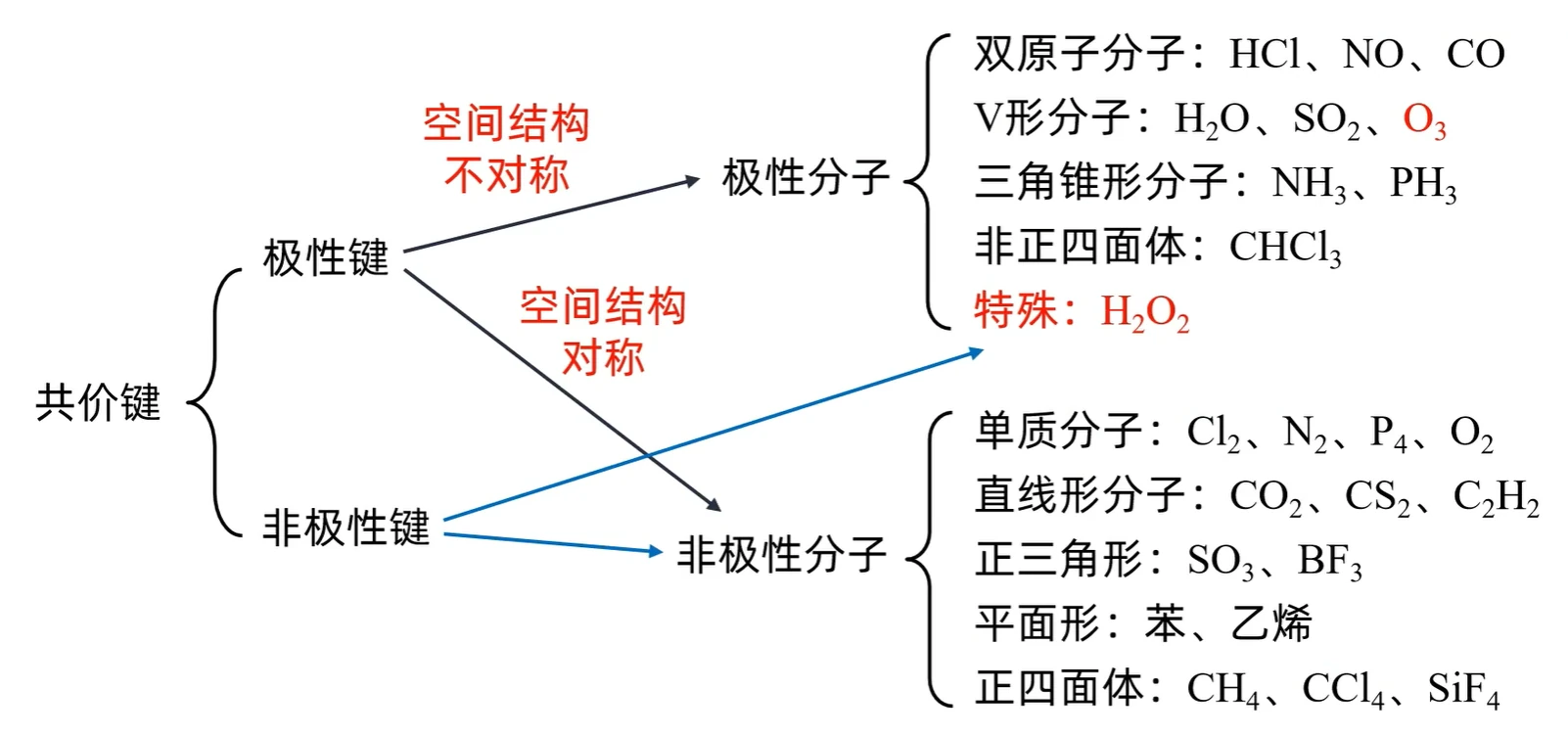
键的极性对化学性质的影响
键的极性对物质的化学性质有重要影响。例如,羧酸是一大类含羧基(
羧酸的酸性可用
不同羧酸的
羧酸 丙酸( ) 乙酸( ) 甲酸( ) 氯乙酸( ) 二氯乙酸( ) 三氯乙酸( ) 三氟乙酸( ) 酸性至上而下由弱变强
三氟乙酸的酸性大于三氯乙酸酸性的原因:由于氟的电负性大于氯的电负性,
三氯乙酸的酸性大于二氯乙酸酸性的原因:由于
甲酸的酸性大于乙酸酸性的原因:烃基(
「相似相溶」规则
非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。如蔗糖、氨、水均是极性分子,
相似相融规则是一条经验规则,并不绝对,如
既不溶于水,也难溶于苯
- 内因
- 物质自身的结构,「相似相溶」还适用于分子结构的相似性。如低级醇(甲醇、乙醇等)可以与水以任意比互溶,而戊醇的烃基较大,其中的一个
与水分子的一个 的相似因素小得多,在水中的溶解度明显减小 - 如果溶质和溶剂之间形成氢键,则溶质在溶剂中的溶解度比较大。如果溶质分子不能与水分子形成氢键,则在水中的溶解度就比较小
- 化学反应—溶质与溶剂反应可增大溶解度。如
与 反应生成 等。
- 物质自身的结构,「相似相溶」还适用于分子结构的相似性。如低级醇(甲醇、乙醇等)可以与水以任意比互溶,而戊醇的烃基较大,其中的一个
- 外因
- 温度:一般来说,温度升高,固体物质的溶解度增大,气体物质的溶解度减小
- 压强:压强越大,气体的溶解度越大
分子的手性
- 手性异构体与手性分子
具有完全相同的组成和原子排列的一对分子,如同左乎和右手一样互为镜像,在三维空间里不能叠合,互称手性异构体或对映异构体。有手性异构体的分子称为手性分子 - 手性分子的判断
在一个有机物分子中,如果有 1 个碳原子分别连有个不同的原子或基团,则该碳原子称为手性碳原子。名有手性碳原子的有机物分子即为手性分子。手性碳原子是产生手性的重要判断依据。 - 手性分子的用途
- 构成生命体的有机分子绝大多数为手性分子。互为手性异构体的两个分子的性质不同
- 生成手性药物、手性催化剂(手性催化例只催化或主要催化一种手性分子的合成)