硫及其化合物
- 游离态:硫单质俗称硫黄,主要存在于火山口附近或地壳的岩层中
- 化合态:主要以 硫化物 和 硫酸盐 的形式存在
黄铁矿 黄铜矿 生石膏 熟石膏 芒硝 的常见化合价: (无 价)
硫单质
物理性质
- 色态:黄色晶体,质脆,易研成粉末
- 溶解性:难溶于水,微溶于酒精、乙醚,易溶于二硫化碳
,易溶于热煤油(化工题常考) 因此二硫化碳可用于洗涤内壁附着硫单质的试管
浓氢氧化钠溶液可以与硫单质反应:
,也可用于除去S
化学性质
硫单质既表现 氧化性 ,又表现 还原性
- 与
硫化氢,
- 与
点 燃 无论氧气是否过量,产物均为二氧化硫(三氧化硫只在特殊的催化条件下生成)。发出明亮的蓝紫色火焰
- 与金属反应
、 用于覆盖实验室撒落的汞以处理汞。
硫酸
物理性质
纯硫酸是无色、黏稠的油状液体,沸点高、难挥发。常用的浓硫酸的质量分数是
化学性质
- 难挥发性:用于制备挥发性酸(如
、 浓 浓 - 强酸性
制磷酸:浓 > 一般使用 $70\%$ 的浓硫酸,因为 $98\%$ 的浓硫酸氢离子浓度过小 - 吸水性
浓硫酸具有 强烈的吸水能力 ,能 吸收空气中的水分 ,甚至能 吸收结晶水合物的水 ,故浓硫酸常用作 干燥剂 ,干燥一些 不与浓硫酸反应的气体 。用浓
、 、 、 、 、 、 、 、 、 酸 碱 反 应 、 、 氧 化 还 原 运用:在乙酸乙酯的制备实验中,用浓硫酸吸水,促进反应正向移动,提高乙酸乙酯的产率
- 脱水性
浓硫酸具有很强的腐蚀性,能按氢、氧原子- 蔗糖的脱水实验:
浓 浓
既体现浓硫酸的 脱水性 又体现 强氧化性
- 醇的消去反应:
浓
- 蔗糖的脱水实验:
- 强氧化性
硫酸中的硫元素处于最高价态。浓硫酸 能与许多物质发生氧化还原反应,是常见的氧化剂- 与铜反应:
浓 不浓不热不反应
- 与木炭反应:
浓
- 与铜反应:
- 其他
- 在常温下,浓
、 、 、 - 金属单质或低价金属的盐与浓
- 在常温下,浓
二氧化硫
物理性质
无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(1 体积的水能溶解约 40 体积的二氧化硫),可用于杀菌消毒和防氧化(向葡萄酒中加入适量二氧化硫)
化学性质
Ⅰ
- 与水反应:
完 全 - 与碱反应:
- 少量
- 过量
- 少量
- 制备:
浓
Ⅱ
- 还原性
- 二氧化硫在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成三氧化硫
三氧化硫也是一种酸性氧化物,溶于水时与水发生剧烈反应,生成硫酸
应用:工业制备硫酸(接触法制硫酸)
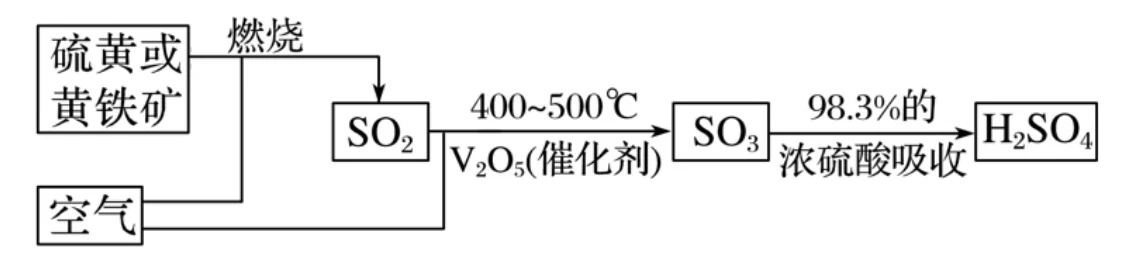
工业上一般以硫磺(
高 温 点 燃 (一般工业上不用水吸收三氧化硫,而是使用98%浓硫酸,因为三氧化硫溶于水大量放热,水沸腾形成酸雾,酸雾随着气流离开,减少对三氧化硫的吸收效果)
- 能被
、 、 、 、 、 、 、 二氧化硫不与浓硫酸反应,因为两者如果反应,会归中反应至+5 价,而+5 价的硫化物不稳定
因此,二氧化硫可以用浓硫酸干燥
- 二氧化硫在适当的温度并有催化剂存在的条件下,可以被氧气氧化,生成三氧化硫
- 氧化性
- 漂白性
- 漂白的原理是
- 工业上常用
- 将
- 氯水的漂白原理与
- 将氯水与
- 将
- 不加热型制备
反应原理:浓
离子方程式:一般使用
- 加热型制备
浓 常考有关阿伏伽德罗常数问题,无法根据
- 干燥:使用浓
- 收集:密度比空气大,向上排空气法
- 尾气处理:
- 物理性质:标况下为无色固体,常温下为无色液体,熔点为
- 化学性质:
- 与水反应:
- 与碱性氧化物反应
- 与碱反应:
- 与某些盐溶液反应:
用于鉴别
- 与水反应:
硫酸根离子的检验
- 原理:在溶液中,
强酸根形成的沉淀往往难溶于强酸,例如
拓展:
浓 - 操作方法
- 取少许待测液于洁净试管中,先加入足量稀盐酸酸化
、 、 、 、 - 上一步后无明显现象(若有沉淀,则静置后取上层清液),滴加
- 若有白色沉淀产生,则说明待测液中含有
若无白色沉淀产生,则说明待测液中不含
- 取少许待测液于洁净试管中,先加入足量稀盐酸酸化
- 注意事项
- 不能只加入
例如:待测液先加入
因为虽然排除了
- 不可以引入硝酸根,例如不可以加
- 不能只加入
硫及其化合物的转化
其他含硫化合物
1、
- 制备:
需 长 时 间 煮 沸 - 性质:
- 酸性条件下歧化:
- 还原性:可被碘氧化(碘量法的原理):
连 四 硫 酸 根 - 与氧气反应:
- 无氧条件下分解:
- 酸性条件下歧化:
2、
- 制备:无氧条件下用锌粉还原亚硫酸氢钠:
- 性质:其可看作是
被潮湿空气氧化:
3、
- 制备:由
- 性质:
- 与酸反应生成
- 强还原性:
- 与酸反应生成
4、
- 性质:与水反应生成硫酸:
5、
- 制备:
- 分解:
- 用途:用作熔矿剂
6、
- 性质:阴离子中含一个过氧键(
- 氧化性:
- 不稳定,遇热易分解:
- 氧化性: