元素及其化合物
硅及其化合物
介绍硅单质的结构和性质、与非金属的反应,以及二氧化硅的结构、物理性质和化学性质。
单晶硅
- 单晶硅的结构与金刚石的相似,为正四面体的立体网状结构。晶体中每个
原子与其他 个 原子相连接 - 单晶硅是带有金属光泽的灰黑色固体,熔点高、硬度大、有脆性,在常温下化学性质不活泼
- 单晶硅的导电性介于导体和绝缘体之间,是良好的半导体材料
化学性质
- 与非金属单质反应
与 都可以和 反应生成 ,而且前者是非金属,后者是金属。在元素推断题中常出现 高 温 金 刚 砂
- 与水反应
- 野外制氢:
- 野外制氢:
二氧化硅
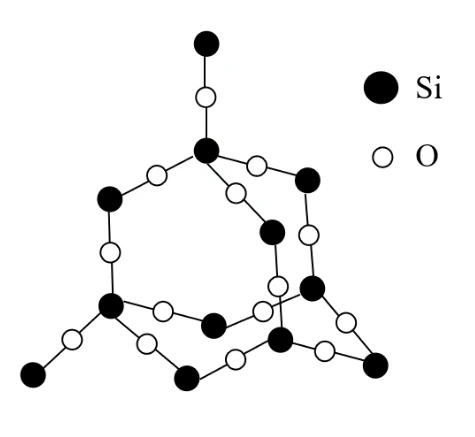
- 结构
- 杂化方式:
- 在
- 在
- 在
- 在
- 硅原子个数与
- 杂化方式:
- 物理性质
- 硬度大、熔沸点高、常温下为固体、难溶于水、不导电
- 化学性质
- 与强碱反应:
- 与唯一一种能与之反应的酸———氢氟酸 反应:
- 与碱性氧化物反应:氧化硅与碱性氧化物反应,不与水反应(与水反应产物为硅酸,是沉淀,阻止反应进行)
- 与碱性盐反应
高 温 高 温 高 温
- 与碳反应
高 温 高 温
- SiO2的精炼
高 温
- 高纯硅(9N+)的制备
- 与强碱反应:
硅酸
- 白色胶状沉淀
- 弱酸性
不使酸碱指示剂变色,酸性小于碳酸 - 不稳定性
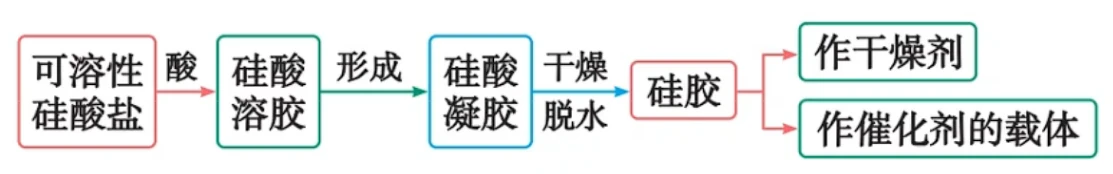
- 硅酸浓度大时在水中易聚合形成透明、胶冻状的硅酸凝胶,硅酸凝胶经干燥脱水后得到多孔的硅酸干凝胶,成为“硅胶”
硅胶是多孔状,吸附水分子能力强,常用作(食品级)干燥剂,或作催化剂的载体 - 向硅酸盐溶液中加入盐酸或通入
胶 体 制备硅酸的原理是“强酸制弱酸”,这一原理可用来设计酸性强弱比较的实验,如:证明盐酸 > 碳酸 > 硅酸
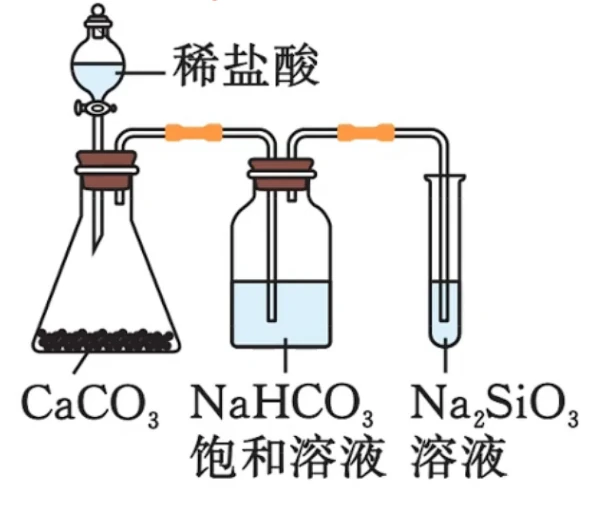
- 注意:该实验不能用于验证非金属性
硅酸钠
最简单的硅酸盐
- 白色、可溶于水的粉末状固体,其水溶液俗称水玻璃、泡花碱,是一种矿物胶,有很强的粘合性(所以装
- 可以与酸(盐酸、碳酸等)反应,生成硅酸凝胶
- 用途:制备硅胶,作木材、纺织品的防腐剂、防火剂